 |
ATLANTA, 11 Ogos 2022 /PRNewswire/ -- Frontier Biotechnologies, sebuah syarikat biofarmaseutikal yang memberi tumpuan kepada penemuan, pembangunan dan penyebaran ubat-ubatan inovatif yang meningkatkan kesihatan pesakit, mengumumkan keputusan positif daripada percubaan klinikal Fasa 1 calon ubatnya, FB2001 – perencat molekul kecil protease utama coronavirus (Mpro) – dalam kalangan sukarelawan dewasa yang sihat.
Data tersebut, dibentangkan di sesi poster Persidangan Antarabangsa berhubung Penyakit Berjangkit Baru Muncul (ICEID) ke-11 menunjukkan bahawa FB2001 selamat dan diterima dengan baik dalam kalangan peserta percubaan. Kejadian buruk dilaporkan semasa percubaan kebanyakannya ringan hingga sederhana dari segi keterukan, dengan tiada perbezaan ketara dilihat antara peserta-peserta di pusat kajian Cina dan Amerika.
"Kami berasa gembira dengan keputusan positif daripada percubaan fasa 1 FB2001. Ia merupakan pencapaian yang signifikan buat kami dan komuniti penjagaan kesihatan," kata Dr CJ Wang, Ketua Pegawai Eksekutif Frontier Biotechnologies. "Keputusan yang memberi harapan ini akan mendorong kami untuk berusaha mencapai kejayaan dalam percubaan peringkat seterusnya. Kami percaya kerja yang dilakukan di Frontier Biotech dapat mempertingkatkan usaha kami dalam perjuangan memerangi COVID-19 di China dan luar negara."
Sejumlah 120 peserta (80 golongan ketuanan kulit putih di AS dan 40 orang Cina di China) menerima infusi intravena FB2001 sama ada satu dos daripada 5 mg hingga 400 mg atau beberapa dos iaitu 30 mg hingga 400 mg setiap hari selama 5 hari. Penemuan penting daripada kajian tersebut adalah seperti berikut:
Keputusan daripada percubaan Fasa 1 adalah berasaskan data in vivo praklinikal FB2001, yang mana ubat tersebut dilihat mengurangkan beban virus dalam tisu paru-paru mahupun otak tikus. Data farmakokinetik yang diperoleh daripada kajian-kajian praklinikal menunjukkan kepekatan FB2001 yang jauh lebih tinggi dalam paru-paru berbanding plasma. "FB2001 telah menunjukkan aktiviti antivirus in vivo dalam tisu paru-paru dan otak bagi model tikus SARS-CoV-2 tanpa memerlukan penggalak farmakokinetik. Justeru itu, ia mempunyai potensi yang besar sebagai rawatan untuk COVID-19 akut serta COVID jangka panjang, yang mana kedua-duanya akan dinilai dalam kajian-kajian susulan yang selanjutnya," kata Dr Jay Lalezari, MD, Pengarah Perubatan Quest Clinical Research di San Francisco.
Formulasi intravena semasa FB2001 ideal untuk pesakit yang dimasukkan ke hospital dengan permulaan tindakan yang pantas dan sesuai untuk pesakit yang mengalami disfagia atau masalah-masalah menelan yang lain. Bekerjasama dengan pertubuhan penyelidikan klinikal, agensi kawal selia serantau dan pusat klinikal tempatan, Frontier Biotechnologies memulakan kajian Fasa 2/3 yang utama (percubaan BRIGHT) untuk mendaftarkan kira-kira 1,200 pesakit yang dimasukkan ke hospital di beratus-ratus pusat klinikal seluruh dunia. "Data fasa 1 benar-benar menunjukkan harapan," kata Dr Michael Hu, Ketua Pegawai Perubatan Frontier Biotechnologies, "dan kami yakin untuk menjalankan percubaan penting ini bagi meninjau utiliti ubat tersebut dalam mengurangkan masa pemulihan dalam kalangan pesakit yang dimasukkan ke hospital ekoran COVID-19."
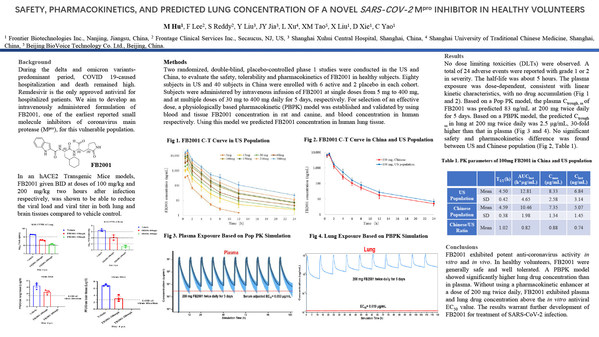
Poster yang dibentangkan di Persidangan Antarabangsa berhubung Penyakit Berjangkit Baru Muncul (ICEID) ke-11
Frontier Biotechnologies turut membangunkan formulasi pulmonari FB2001 yang boleh digunakan dalam persekitaran pesakit luar untuk rawatan Covid-19 ringan, selain untuk profilaksis selepas pendedahan. Apabila disedut terus ke dalam saluran pernafasan dan paru-paru, kepekatan FB2001 dalam tisu adalah jauh lebih tinggi berbanding dalam plasma; justeru itu, permulaan tindakan dan pembersihan virus berpotensi menjadi lebih pantas berbanding terapi oral.
Latar Belakang Frontier Biotechnologies
Ditubuhkan pada tahun 2013, Frontier Biotechnologies Inc. ("Frontier Biotech") ialah sebuah syarikat biofarmaseutikal tahap komersial yang beribu pejabat di China dengan visi global dan daya saing bertaraf dunia. Frontier Biotech komited terhadap penemuan, pembangunan, pembuatan dan pengkomersialan ubat-ubatan inovatif yang meningkatkan kesihatan pesakit.